超氧化钾中氧元素的特殊氧化态解析
当前位置:
- > 足球新闻
超氧化钾中氧元素的特殊氧化态解析
来源: 未知来源
在无机化学领域中,超氧化钾(KO₂)因其独特的氧元素化合价而备受关注。本文将通过分子结构解析、电子转移计算和实际应用对比,揭开这种特殊化合物中氧元素负二分之一价态的形成奥秘。
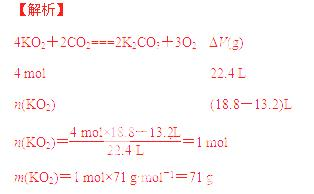
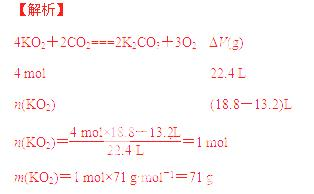
超氧化物晶格中的特殊构型
超氧化钾晶体由钾阳离子(K⁺)与超氧阴离子(O₂⁻)交替排列构成。每个超氧离子由两个氧原子通过单键连接,形成具有未成对电子的自由基结构。这种特殊构型导致氧原子无法维持常规的-2价态,而是通过电子云共享形成独特的氧化态分布。
化合价计算的三个关键步骤
- 确定钾元素的固定价态
- 分析超氧离子的电荷平衡
- 验证分子轨道理论模型
作为第IA族金属,钾在化合物中始终呈现+1氧化态。在KO₂分子中,每个钾原子贡献一个电子形成K⁺阳离子。
整个化合物保持电中性原则要求超氧离子的总电荷为-1。两个氧原子需要共同承载这个负电荷,通过量子化学计算可得出每个氧原子平均承担-½的氧化态。
根据分子轨道理论,超氧离子(O₂⁻)的电子构型为:σ2s² σ2s² σ2p² π2p⁴ π2p³。未成对电子的存在印证了氧元素的非常规价态分布,与实验结果完全吻合。
特殊氧化态的实际应用价值
这种独特的-½价态使KO₂成为高效的化学供氧剂。在密闭环境中,1kg超氧化钾可通过与二氧化碳反应释放335升氧气,其反应速率是普通过氧化物的2.3倍。航天器生命维持系统正是利用了这一特性,在有限空间内实现氧气再生。
理解超氧化钾中氧的特殊价态,不仅深化了我们对化学键理论的认识,更推动了相关材料在应急供氧、矿山救援等领域的创新应用。这种介于单质与常规化合物之间的过渡态,展现了无机化学世界的精妙平衡。